+86 13683842418
+86 13683842418
河南省洛阳市洛阳国家大学科技园
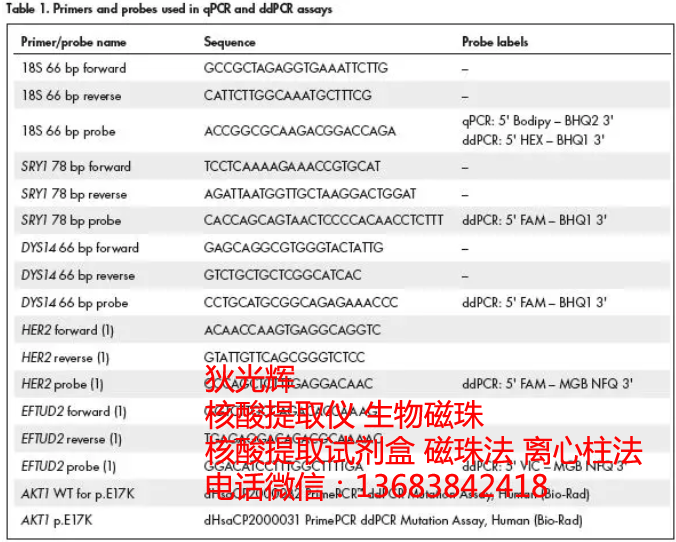
在评估过程中,首先对待提取的血浆样本中加入了经梯度稀释的低丰度生物标记物作为对照,然后将最高达10 ml的这些不同血浆样本利用QIAsymphony SP全自动核酸纯化仪进行游离DNA的自动化提取,最后利用Qubit、qPCR和ddPCR等不同方法对提取得到的游离DNA进行质控及定量分析。在qPCR和ddPCR的检测过程中,针对人类18S rRNA编码区域而设计的引物及探针将用于游离DNA的定量,并针对男性特殊的游离DNA也设计了一组针对Y染色体特异性多拷贝基因DYS14及单拷贝基因SRY1的引物及探针,而对于突变(AKT1 E17K)及拷贝数(HER1)检测的引物探针体系也被加入设计用于后续的检测实验。
对来自对位健康男性及女性志愿者的10 ml全血样本按照标准操作流程进行血浆的分析,并将其中的男性血浆(0-1024 ul范围)按照一定的梯度加入至相应体积女性血浆中,使得最终的总血浆体积为2 ml。随后,利用QIAsymphony DSP Circulating DNA Kit在自动化平台上对血浆样本(四组重复)中的cfDNA进行提取后采用ddPCR对Y染色体特异性基因标记进行定量检测,并利用其中多拷贝基因DYS14及单拷贝基因SRY1的数据确定最低的检出下限 (LoD),确保在大量正常cfDNA背景条件下也能对特殊的低丰度cfDNA片段进行有效的检测。
首先,对提取得到的cfDNA利用Qubit(dsDNA HS Assay Kit)及经验证的实时定量PCR系统(针对18S rDNA的一段66 bp扩增产物)进行定量分析。从检测结果来看,QIAsymphony DSP Circulating DNA Kit(下图中蓝点))能够很好的将1-10 ml起始血浆样本的游离DNA进行极为有效且稳定的提取,并与采用经典手工方法(4 ml血浆8组重复,下图中红点)提取得到的结果高度吻合。
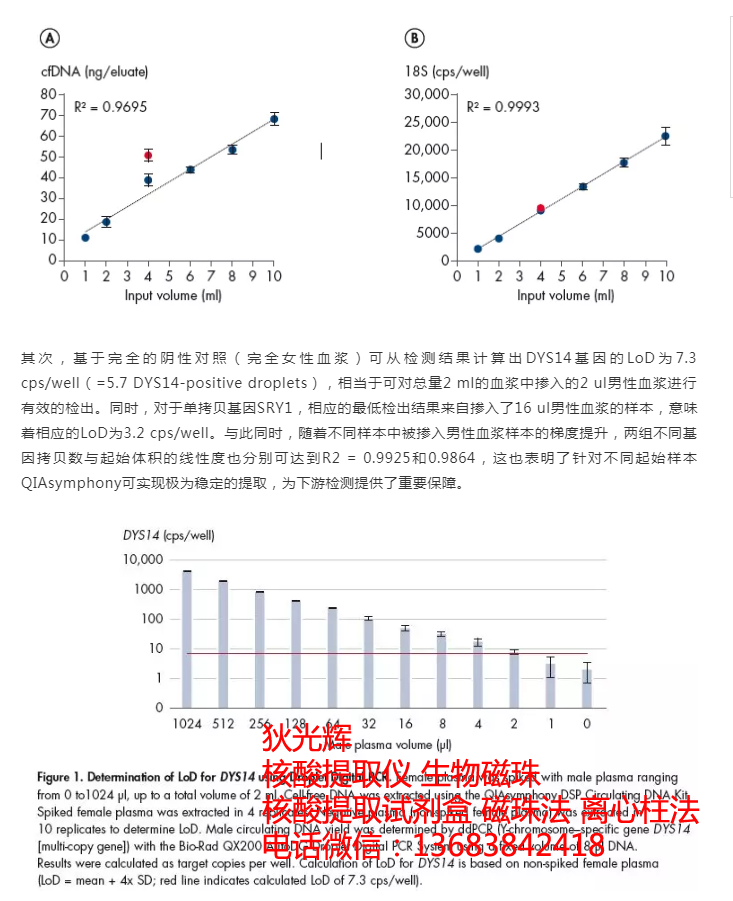
其次,基于完全的阴性对照(完全女性血浆)可从检测结果计算出DYS14基因的LoD为7.3 cps/well(=5.7 DYS14-positive droplets),相当于可对总量2 ml的血浆中掺入的2 ul男性血浆进行有效的检出。同时,对于单拷贝基因SRY1,相应的最低检出结果来自掺入了16 ul男性血浆的样本,意味着相应的LoD为3.2 cps/well。与此同时,随着不同样本中被掺入男性血浆样本的梯度提升,两组不同基因拷贝数与起始体积的线性度也分别可达到R2 = 0.9925和0.9864,这也表明了针对不同起始样本QIAsymphony可实现极为稳定的提取,为下游检测提供了重要保障。
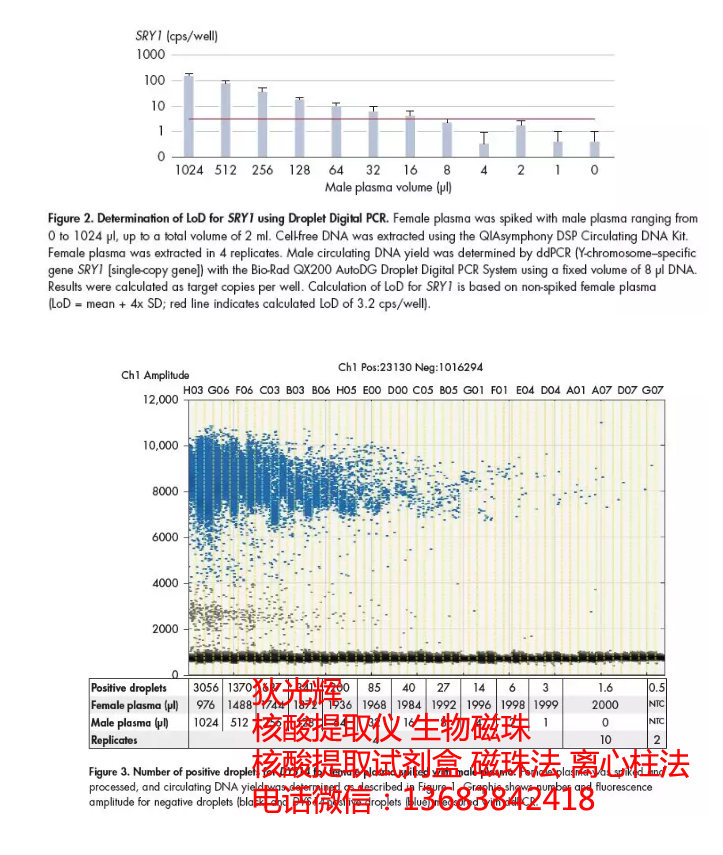
在由客户提供的一组真实样本检测结果中,我们可以看到QIAsymphony Circulating DNA系统所提取得到的cfDNA可支持突变频率最低至0.08%的超灵敏检测。在此项研究中,作者对来自相应供体中4-8 ml的血浆样本采用QIAsymphony系统进行了自动化提取,并对AKT1 E17K点突变以及HER2的扩增突变利用数字PCR进行了检测。
在AKT1 E17K体细胞突变检测中,来自8 ml临床血浆中的cfDNA经提取后用120 ul洗脱液进行洗脱,基于0.469 ng/ul的Qubit定量浓度采用7.5 ul DNA溶液(cfDNA总量相对于0.5 ml血浆样本中的含量)进行ddPCR分析。从结果可以看出,Y轴上的荧光信号所代表的蓝色突变液滴数 (10),与X轴上的荧光信号所代表的绿色野生型液滴数 (666) 表明突变存在的频率为1.5%。与此同时,对另外一组血浆样本的提取结果这两个采用10 ng cfDNA(相当于2 ul DNA洗脱液)进行HER2检测,可得到4.75倍 (3155:727) 的扩增比例检出结果。
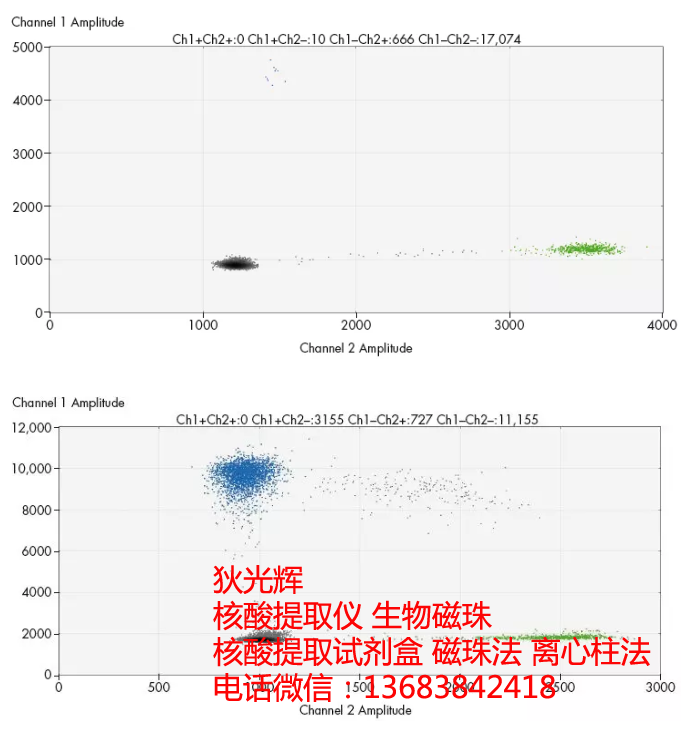
以上结果表明,作为一种高通量自动化提取方法,QIAsymphony DSP Circulating DNA Kit在QIAsymphony提取平台的支撑下可实现极为高效稳健的提取,在传统PCR、NGS等技术平台方法之外,还能有效的为数字PCR针对极低丰富标志物的检测提供有力保障。
目前,QIAsymphony DSP Circulating DNA Kit已获得国家药品监督管理局第一类医疗器械备案凭证用于临床诊断过程样本制备,期待来自QIAGEN的游离核酸检测方法为您提供强有力的支持。