+86 13683842418
+86 13683842418
河南省洛阳市洛阳国家大学科技园
2017年6月22日,BLOOD在线发表的一篇文章中,报道了 Gardner等研究人员使用嵌合抗原受体(CAR)T细胞疗法治疗儿童和青少年复发难治性B细胞急性淋巴细胞白血病(r/r B-ALL)的临床一期试验结果:12个月无病生存率为50.8%,总体生存率为69.5%,微小残留疾病(MRD)阴性缓解率为89%。
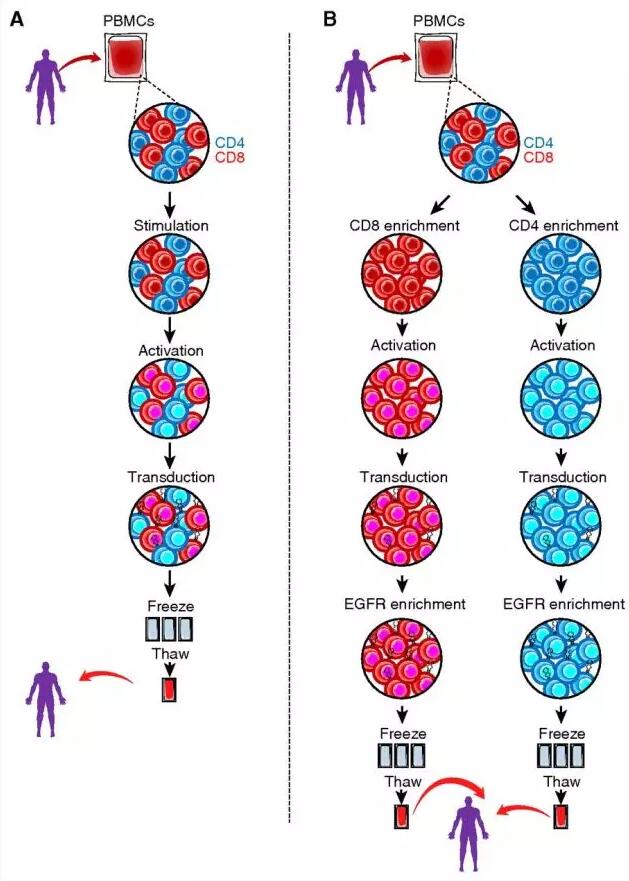
试验方案
该试验招募45例患者入组,接受经慢病毒转染的CD4/CD8比例明确的抗CD19-41BB CART细胞治疗。
在试验中,研究人员通过一种特定的制备工艺使CART细胞中CD4/CD8比例固定,提高外源基因转染、表达水平,并减弱T细胞的分化。
研究人员采用免疫磁珠分离法将CD4+/CD8+T细胞从外周血中分离出来,富集后用CD3/CD28磁珠分别刺激这些确定数量的CD4/CD8T细胞,携带EGFRt基因的抗CD19 CAR慢病毒载体转染T细胞,并通过稳态因子限制由激活介导的细胞分化。CD4培养辅以IL-7、IL-5,CD8培养辅以IL-15和IL-2。最终,去除CD3/CD28磁珠颗粒,用CliniMACS阳性分选出表达EGFRt的细胞。
图A展示的是更为标准化的CART制备工艺:由缺少上述分选、富集步骤的大量T细胞群来制备CART细胞。
图B展示了Gardner等的研究所采用的制备工艺,此工艺源于一项临床前研究结论,即:
(1)CD4与CD8按1:1的比例混合
(2)培养环境添加合适的稳态因子
这样能最大程度的发挥出两种T细胞群的效能(保持最大程度的细胞杀伤能力;延长体内存留时间;维持细胞记忆和自我更新功能),并且减少记忆T细胞的终末分化。
研究结果
93%的入组患者接受了CART细胞回输,总体意向治疗(ITT)分析显示,微小残留疾病(MRD)阴性缓解率为89%。
值得注意的是,所有接受氟达拉滨-环磷酰胺联合化疗预处理的患者,都达到了MRD阴性缓解。这说明,在抗CD19 CART细胞回输前,通过氟达拉滨联合环磷酰胺所进行的淋巴扫除术,是非常必要的。
试验并无致死情况发生,副作用近似或优于其他已报道的抗CD19 CART细胞临床试验研究。23%的患者经历了严重的细胞因子释放综合征(CRS)和/或可逆的重度神经毒性事件。
长期随访结果显示,12个月无病生存率为50.8%,总体生存率为69.5%。这与之前宾夕法尼亚大学(Penn)和美国国家癌症研究院(NCI)开展的抗CD19 CART细胞治疗儿童ALL临床试验中报告的反应率近似。
18例复发病例中,7例与CD19的表达缺失有关,而功能性CART细胞的缺失是CD19+肿瘤复发的危险因素之一,其发生率与其他已报道的抗CD19 CART细胞的研究近似。
讨论
1、研究人员认为,试验显示的良好的ITT MRD阴性缓解率和总体生存率主要归因于研究中使用的T细胞产品。研究尝试了大量方法来进一步提高CART细胞的功效,例如:
(1)使用不同的胞内共刺激基序(较为典型的是CD28或4-1BB)以增强T细胞的活性及延长细胞寿命
(2)对间隔区或铰链区结构进行修饰
正如在Gardner和其他人的文章中提到的,细胞所处细胞因子环境和最适宜CAR转染及制备的T细胞表型,也是影响CART细胞临床研究的重要因素。比较复杂的是,患者个体间的差异性,例如年龄、绝对淋巴细胞计数(ALC)、之前用的治疗方法等,都会影响到T细胞产品的质量。
然而,在不同的制备技术、不同的慢病毒或逆转录病毒载体和胞内共刺激区等条件下制备出的抗CD19 CART细胞在治疗r/r ALL的临床研究中,都能展现出良好的治疗效果。因此,辨别出何种因素决定抗CD19 CART细胞体内存留时间和抗肿瘤活性,是目前临床研究面临的挑战之一。
到目前为止还无法证实Gardner等的研究结论,这种更为复杂且花费更高的工艺的有效性,有赖于患者的反应率和生存率数据的支持;并且,是否接受不同的抗CD19 CART细胞产品治疗的患者会出现长期生存率上的差异,需要对更多的患者进行长期跟踪随访。
2、另一个重要的发现是,在出现MRD(正常及恶性CD19+B细胞数量较少)的患者体内,抗CD19 CART细胞的扩增较差,体内存留时间较短。正如作者指出的,靶向抗原的缺失这一问题,将会给CART疗法应用于临床一线治疗或合并后作为MRD治疗方法带来挑战。一些研究小组正在探索解决这一潜在缺点的其他方法,包括:
(1)构建多靶向CART细胞
(2)或是在CART细胞回输时提供额外的抗原疫苗
尽管Gardner等的研究中使用的多步骤制备工艺较为复杂,但其成功率很高,并且值得赞扬的是,他们的研究结果是严格基于ITT分析的。之前的研究证实,很难知晓有多少患者由于ALC水平不达标或所制备免疫细胞未放行而临床脱组。
结论
抗CD19 CART细胞疗法正越来越趋向于获得监管部门的上市批准,而其生产工艺的流水线化将是一大关键。这将有助于减少耗材的成本,并建立针对所有产品的测定标准化ITT反应率的方法学。(这样便能判定类似于Gardner等的研究中所用的附加工艺是否有益)
提高细胞制备的成功率,并让抗CD19 CART细胞疗法惠及更多患者,这是无数科研工作者孜孜以求的目标,而这一制备工艺的创新——将CD4和CD8 T细胞进行分离,并在优化的稳态因子环境中分别培养,也许能对此大有裨益。
免疫磁珠:www.ex-dna.com